Краткое содержание
Апикальный периодонтит - это следствие эндодонтической инфекции, которое проявляется в виде защитной реакции организма на микробиологическую угрозу исходящую из системы корневых каналов. Он рассматривается, как динамическое столкновение между бактериальными факторами и защитными силами организма на стыке между инфицированной корневой пульпой и периодонтальной связкой, что выражается в локальном воспалении, резорбции твердых тканей и, в конечном итоге, в формировании различных гисто-патологических форм апикального периодонтита, обычно называемых периапикальными поражениями.
Лечение апикального периодонтита, как инфекционного заболевания корневого канала, состоит из ликвидации либо существенного снижения количества микробов в корневом канале и предотвращение реинфицирования путем обтурации. Лечение дает крайне высокую степень успеха. Тем не менее, эндодонтическое лечение может потерпеть неудачу. Большинство неудач происходят, когда терапевтические процедуры, в основном технического характера, не достигли соответствующего уровня контроля и ликвидации инфекции. Даже при соблюдении самых высоких стандартов и тщательном следовании процедурам, все ещё возможны неудачи. Это обусловлено наличием в канале зон, которые не могут быть очищены и обтурированы существующим оборудованием, материалами и методами, и, таким образом, возможно сохранение инфекции. В очень редких случаях есть также факторы, расположенные в пределах воспаленных периапикальных тканей, которые могут мешать заживлению поражения после лечения.
Данные о биологических причинах эндодонтической неудачи являются новыми и разрозненны в различных журналах. Эта статья написана с целью предоставления всестороннего обзора этио-патогенеза апикального периодонтита и причин неудачного эндодонтического лечения которые после лечения видны на рентгенограммах как симптоматические очаги радиолюценции (рентгенологического просветления).
(I) ВСТУПЛЕНИЕ
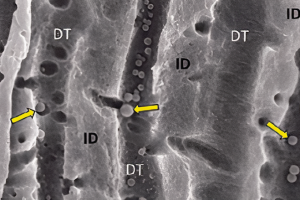
Апикальный периодонтит - это воспалительные и деструктивные изменения в перирадикулярных тканях вызванные этиологическими факторами эндодонтического происхождения. Он, как правило, следствие эндодонтической инфекции (Рис.1). 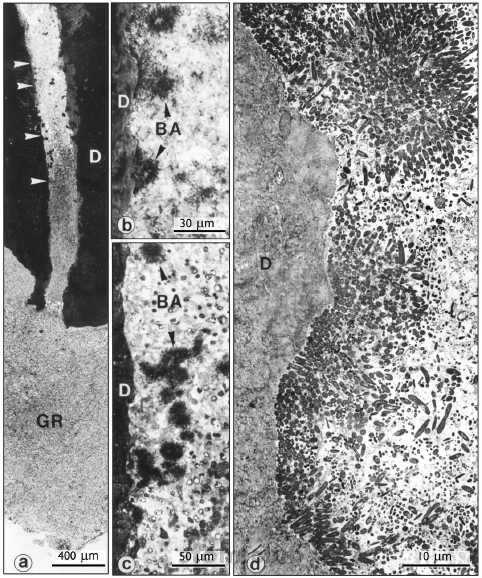
Рисунок 1. Эндодонтческая флора зуба человека с апикальным периодонтитом (GR). Области между двумя верхними и нижними стрелками в (a) увеличены в (b) и (c), соответственно. Обратите внимание на плотные бактериальные аггрегации (BA) прикрепленные (b) к дентинной (D) стенке а так же разведенные среди нейтрофилов в жидкой фазе корневого канала (c). Взгляд через трансмиссионный электронный микроскоп (d) на пульпарно-дентинную границу показывает бактериальное загрязнение на поверхности стенки дентина, формирующее толстую, многослойную биопленку. Увеличение: (a) 46x; (b) 600x; (c) 370x; и (d) 2350x. (From Nair, 1997.)
Изначально, пульпа зуба инфицируется и некротизируется аутогенной микрофлорой полости рта. Эндодонтическое пространство предоставляет селективную среду обитания для возникновения смешанной, преимущественно анаэробной флоры. В совокупности, это адаптированное к окружающей среде полимикробное сообщество, находящееся в корневом канале, имеет несколько патогенных свойств, таких как антигенность, митогенная активность, хемотаксис, ферментативный гистолизис (гистолиз) и активация клеток хозяев. Микрофлора, захватившая корневой канал, может продвигаться либо выводить продукты своей жизнедеятельности, в периапекс. В ответ организм выстраивает защитный строй из клеток нескольких классов, межклеточных мессенджеров, антител и молекул-эффекторов. Микробиологические факторы и защитные силы организма сталкиваются и ведут свою борьбу в периапикальных тканях, приводя к их разрушению, результатом чего становится возникновение различных категорий апикальных поражений. Несмотря на внушительные механизмы защиты, организм не в состоянии уничтожить микроорганизмы базирующиеся в убежище корневого канала, который находится за пределами работы защитных сил организма (Рис.2).
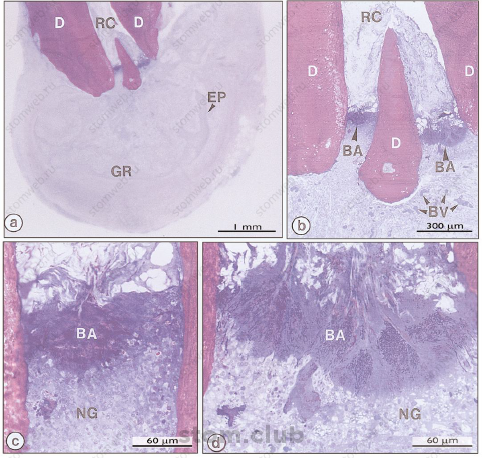
Рисунок 2. Биопленка плотно установившаяся в апикальном отверстии зуба пораженного апикальным периодонтитом (GR). Апикальная дельта в (a) увеличена в (b). Разветвление канала на правый и левый (b) увеличено в (c) и (d), соответственно. Обратите внимание на стратегическое расположение бактериальных кластеров (BA) около апикального отверстия. Бактериальную массу словно удерживает стена нейтрофилов (NG). Очевидно,любые хирургические и/или микробиологические методы отбора проб периапикальных тканей будут загрязнять образцы из внутрекорневой флоры. EP, эпителий. Выходное увеличение: (c) х 20, (b) х 65, (c, d) х 350. (From Nair, 2002.)
Потому, верхушечный периодонтит не заживает сам по себе. Лечение апикального периодонтита состоит из уничтожения инфекции в корневом канале и предотвращения повторного заражения посредством гидравлической пломбировки просвета корневого канала. Несмотря на это, эндодонтическое лечение может провалиться по различным причинам. Патогенез апикального периодонтита был хорошо описан (Stashenko, 1990; Nair, 1997; Stashenko et al., 1998). Тем не менее, даже последние учебники по эндодонтии (Cohen and Burns, 2002; Bergenholtz et al., 2003) не предоставляют обзора причин эндодонтических неудач (на момент написания статьи). Данные о биологических причинах неудач эндодонтического лечения являются новыми, разрозненны по разным журналам, и нуждаются в объединении. Эта статья написана с целью предоставления всестороннего обзора патогенеза апикального периодонтита и причин неудач эндодонтического лечения.
(II) ЭТИОЛОГИЯ АПИКАЛЬНОГО ПЕРИОДОНТИТА
(A) Цепь доказательности
Наличие нескольких отдельных видов бактерий в некротизированой пульпе зуба было продемонстрировано более ста лет назад (Miller, 1890). Существенная роль микроорганизмов в этиологии апикального периодонтита, тем не менее, оставалась неопределенной на протяжении долгих лет. Пол века спустя было доказано (Kakehashi et al., 1965), что апикальный периодонтит не развивается у стерильных крыс-гнатобиотов при вскрытой пульповой камере, в отличии от крыс со стандартной оральной микрофлорой из группы контроля, у которых возникали массивные очаги радиолюценции. Вскоре за тем было признано большое значение облигатных анаэробов в эндодонтической инфекции (Möller, 1966). Эти выводы были подтверждены рядом исследований (Bergenholtz, 1974; Kantz and Henry, 1974; Wittgow and Sabiston, 1975). Было установлено, что корневые каналы 18-ти из 19-ти периапикально поражённых зубов с "интактной" коронковой частью скрывали в себе смесь нескольких видов бактерий, преимущественно состоящих из факультативных анаэробов (Sundqvist, 1976). Серия патобиологических исследований (Fabricius, 1982) впоследствии определила: (а) условия, при которых создается и развивается эндодонтическая микрофлора а так же (б) биологические свойства и эндодонтические условия способствующие патогенизации флоры корневого канала. Экологическая организация микрофлоры в прикрепленные биопленки (рис.1, 2)(скопление(аггрегация) одного или коагрегация нескольких видов микроорганизмов, взвешенных в жидкой фазе инфицированных корневых каналов) была визуализированна с применением точных методов парной световой и трансмиссионной электронной микроскопии (Nair, 1987). Сегодня существует единое мнение о существенной этиологической роли внутриканальных микроорганизмов в протекании апикального периодонтита.
(B) Входные ворота внутриканальной инфекции
Отверстия в стенках твердых тканей зуба (возникающие от кариеса, клинических процедур или от посттравматических переломов и трещин) ,это наиболее распространенные ворота пульпарной инфекции. Но микробы были так же выделены из зубов с некротизированной пульпой и клинически интактными коронками (Brown and Rudolph, 1957; Chirnside, 1957; Macdonald et al., 1957; Engström and Frostell, 1961; Möller, 1966; Bergenholtz, 1974; Wittgow and Sabiston, 1975; Sundqvist, 1976; Baumgartner et al., 1999). Эндодонтической инфекции таких зубов предшествует некроз пульпы. Зуб может казаться клинически интактным, но содержать микротрещины в твердых тканях, которые открывают входные ворота для инфекции. Бактерии из десневой борозды или периодонтальных карманов, как предполагалось, достигали корневых каналов этих зубов через разорванные кровеносные сосуды периодонта (Grossman, 1967). Пульпарная инфекция может также возникать через оголение дентинных тубул цервикальной поверхности корня, из-за наличия щелей в цементном покрытии корня. Так же утверждалось, что микробы могут выпадать на некротизированную пульпу через кровоток (анахорез) (Robinson and Boling, 1941; Burke and Knighton, 1960; Gier and Mitchel, 1968; Allard et al., 1979). Тем не менее, высеять бактерии из корневого канала, когда кровоток был экспериментально инфицирован, не удалось, если только корневые каналы небыли чрезмерно обработаны с, по видимому, повреждением кровеносных сосудов апикального периодонта за период бактериемии (Delivanis and Fan, 1984). В другом исследовании (Möller et al., 1981), все экспериментально девитализированные пультовые камеры обезьян (n = 26) оставались стерильными более 6-ти месяцев. Таким образом, сообщение пульповой камеры с полостью рта - это наиболее важный путь эндодонтической инфекции.
(C) Эндодонтическая флора зубов с первичным апикальным периодонтитом
Современные знания о таксономии флоры инфицированного корневого канала базируются на передовых техниках микробиологического культивирования. Это может вскоре измениться при разумном применении молекулярных генетических техник в эндодонтической микробиологии (Munson et al., 2002). Не смотря на то, что образцы обширной микрофлоры полости рта (Moore and Moore, 1994) могут инфицировать открытую пульповую камеру, культурологическими исследованиями давно установлено, что только определенная подгруппа оральной микрофлоры, состоящая из ограниченного количества видов, систематически выделяется из таких корневых каналов. Внутриканальная микрофлора зубов с клинически интактными коронками, но с некротизированной пульпой и поражённым периапексом, преобладающе представлена (> 90%) облигатными анаэробами (Sundqvist, 1976; Byström and Sundqvist, 1981; Haapasalo, 1989; Sundqvist et al., 1989), как правило относящимися к роду Fusobacterium, Porphyromonas (ранее Bacteroides; Shah and Collins, 1988), Prevotella (ранее Bacteroides; Shah and Collins, 1988), Eubacterium, и Peptostreptococcus. В противоположность, микробный состав корневого канала периапикально пораженного зуба с пульповой камерой сообщающейся с полостью рта, даже в апикальной трети не только отличается от, но и менее преобладающе (> 70%) представлен облигатными анаэробами (Baumgartner and Falkler, 1991). Используя культорологические методы (Hampp, 1957; Kantz and Henry, 1974; Dahle et al., 1996), электронную микроскопию темного поля (Brown and Rudolph, 1957; Thilo et al., 1986; Dahle et al., 1993) и трансмиссионную электронную микроскопию (Nair, 1987), исследователи нашли спирохеты в некротизированных корневых каналах. Культуральные исследования (для обзора, см. Waltimo et al., 2003) и применение сканирующей электронной микроскопии (Sen et al., 1995) показали присутствие грибков в каналах зубов с первичным апикальным периодонтитом. Присутствие внутриканальных вирусов на сегодняшний день доказано только в не воспаленной пульпе зуба у пациентов зараженных вирусом иммуно-дефицита (Glick et al., 1991).
Изобретение метода полимеразной цепной реакции (ПЦР) (Mullis and Faloona, 1987) и его применение в микробиологии позволило находить бактерии через амплификацию их ДНК. Эти молекулярные методы в значительной степени подтвердили присутствие микробиологических видов, ранее обнаруженных и выращенных культорологическими методами (Munson et al., 2002). Они так же облегчили идентификацию трудно на сегодняшний день высеваемых эндодонтических микроорганизмов и их точную таксономическую принадлежность (Munson et al., 2002). Несмотря на то, что использование молекулярных методик может расширить таксономический спектр потенциальной эндодонтической микрофлоры, в настоящее время нет доказательств, что трудно высеваемые микроорганизмы найденные высокочувствительными молекулярными методами, являются жизнеспособными внутриканальными патогенами. Это происходит потому, что молекулярные генетические методы зачастую применяются без необходимых усиленных мер предосторожности и без учета ограничений этих техник (Siqueira et al., 2000; Siqueira and Rôças, 2003).