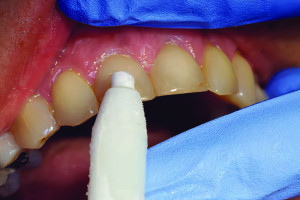
Учитывая, что апикальный периодонтит — это заболевание, вызываемое в первую очередь микроорганизмами и (или) продуктами их метаболизма, поражающими систему корневых каналов, ключом к успеху эндодонтического лечения и заживлению периапикальных тканей является дезинфекция. Известно, что микроорганизмы, агрегированные в биопленки, более устойчивы к воздействиям, и что бактерии, оставшиеся в корневом канале после обтурации, могут поддерживать периапикальный воспалительный процесс. В клиническом исследовании Sjogren et al. подтвердили, что вероятность успеха постэндодонтического лечения была значительно ниже у зубов с апикальным периодонтитом, по сравнению с зубами со здоровыми периапикальными тканями. Следовательно, главной целью эндодонтического лечения хронического апикального периодонтита и длительного инфекционного процесса является дезинфекция системы корневых каналов, которую следует проводить как можно раньше, поскольку апикальный периодонтит вызывает разрушение тканей, включая потерю прикрепления волокон периодонтальной связки, одновременно с резорбцией цемента и кости (Рисунок 1 a, b), что, в свою очередь, приводит к утрате зуба.
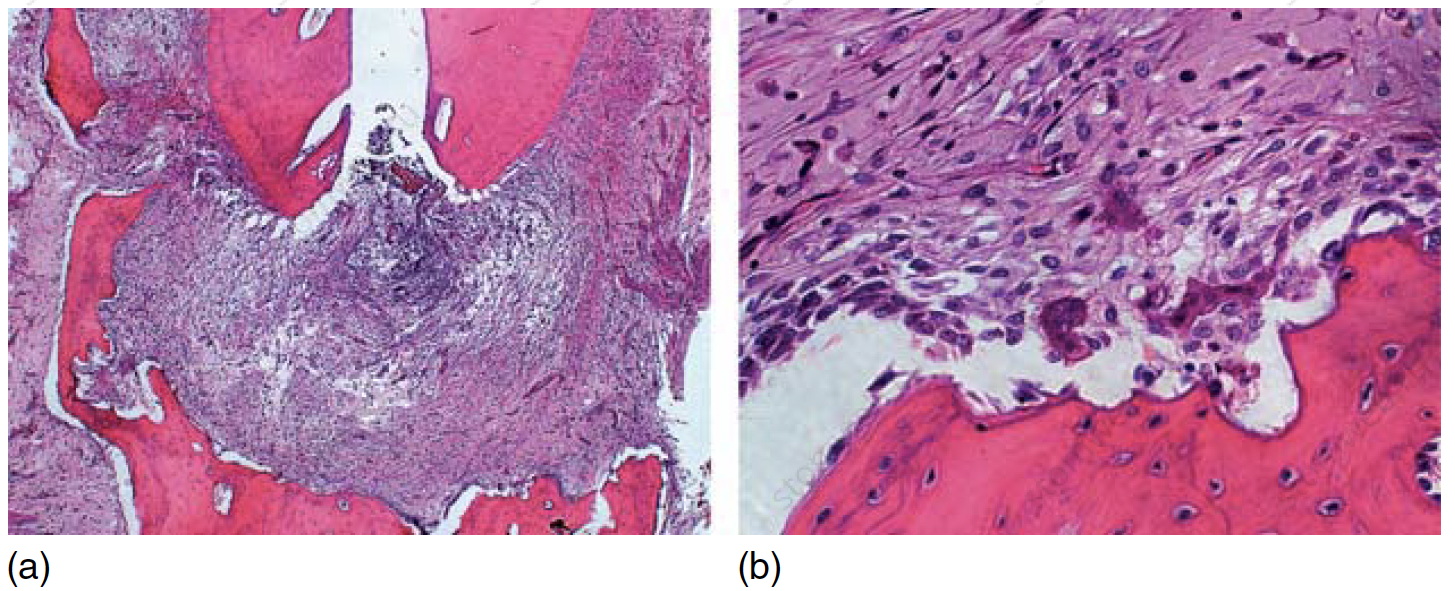
Рисунок 1 (а, b) Апикальный периодонтит: разрушение тканей, потеря прикрепления волокон периодонтальной связки, цемента и резорбция костной ткани. Гематоксилин и эозин.
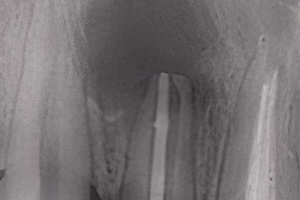
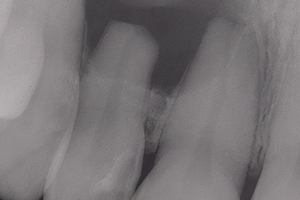
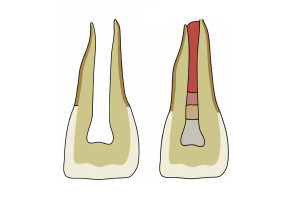
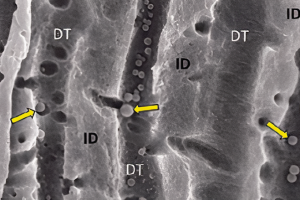
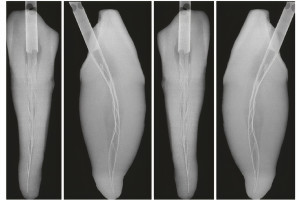
В профессиональной среде давно обсуждается вопрос, может ли сама по себе биомеханическая подготовка (инструментация и ирригация) корневого канала зуба с апикальным периодонтитом уничтожить все микроорганизмы. При проникновении инфекции в эндодонт, микроорганизмы распространяются по всей системе корневых каналов, а именно – по главному каналу, боковым, добавочным и вторичным каналам, дентинным канальцам (Рисунок 2), цементным лакунам (Рисунок 3), разветвлениям апикальной дельты (Рисунок 4 а, b), они проникают в апикальное отверстие, апикальные эрозии и даже организуются в виде биопленок на внешних поверхностях апикальной трети корня (Рис 5 a, b). Эти поверхности представляют собой области, недоступные для механической обработки и иммунной системы организма.

Рисунок 2 Микроорганизмы рассеяны по дентинным канальцам зубов с апикальным периодонтитом. Окрашивание по Брауну и Бренну.
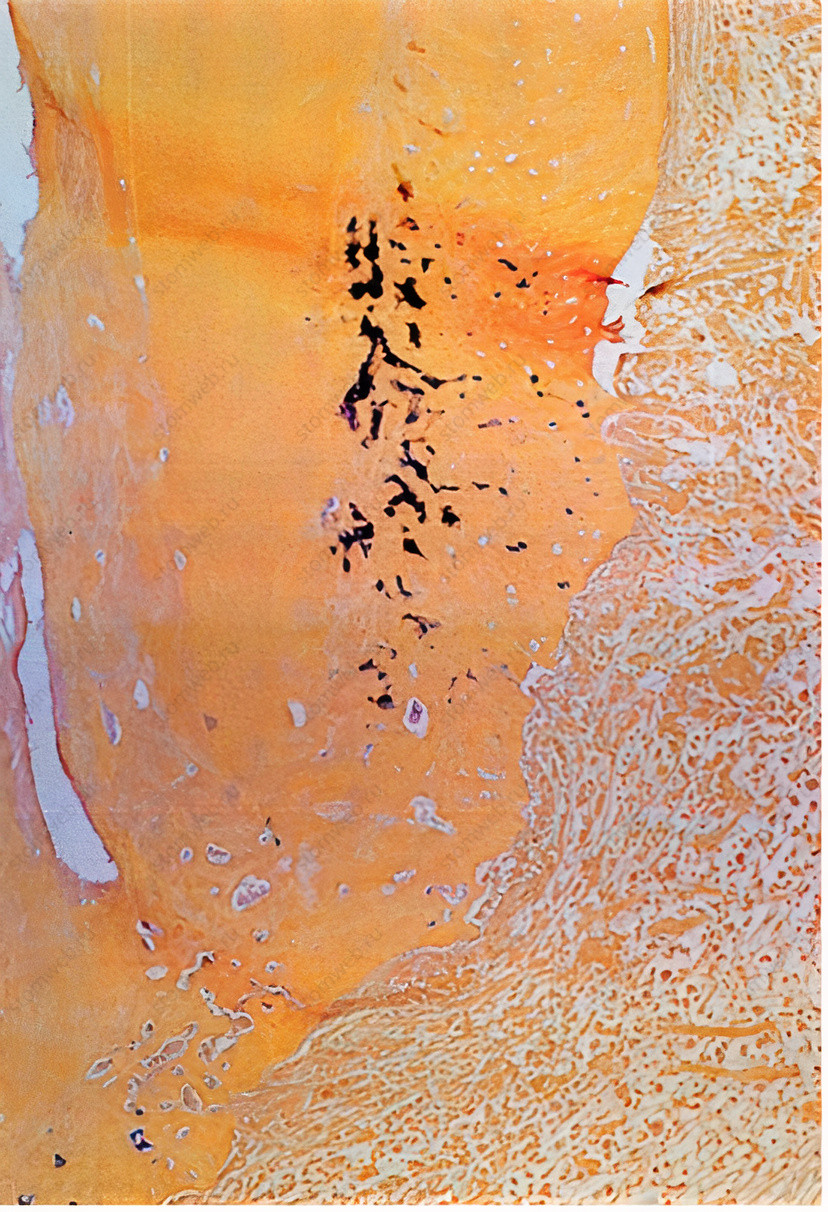
Рисунок 3 Микроорганизмы, обнаруженные в цементных лакунах зубов с апикальным периодонтитом. Окрашивание по Брауну и Бренну.
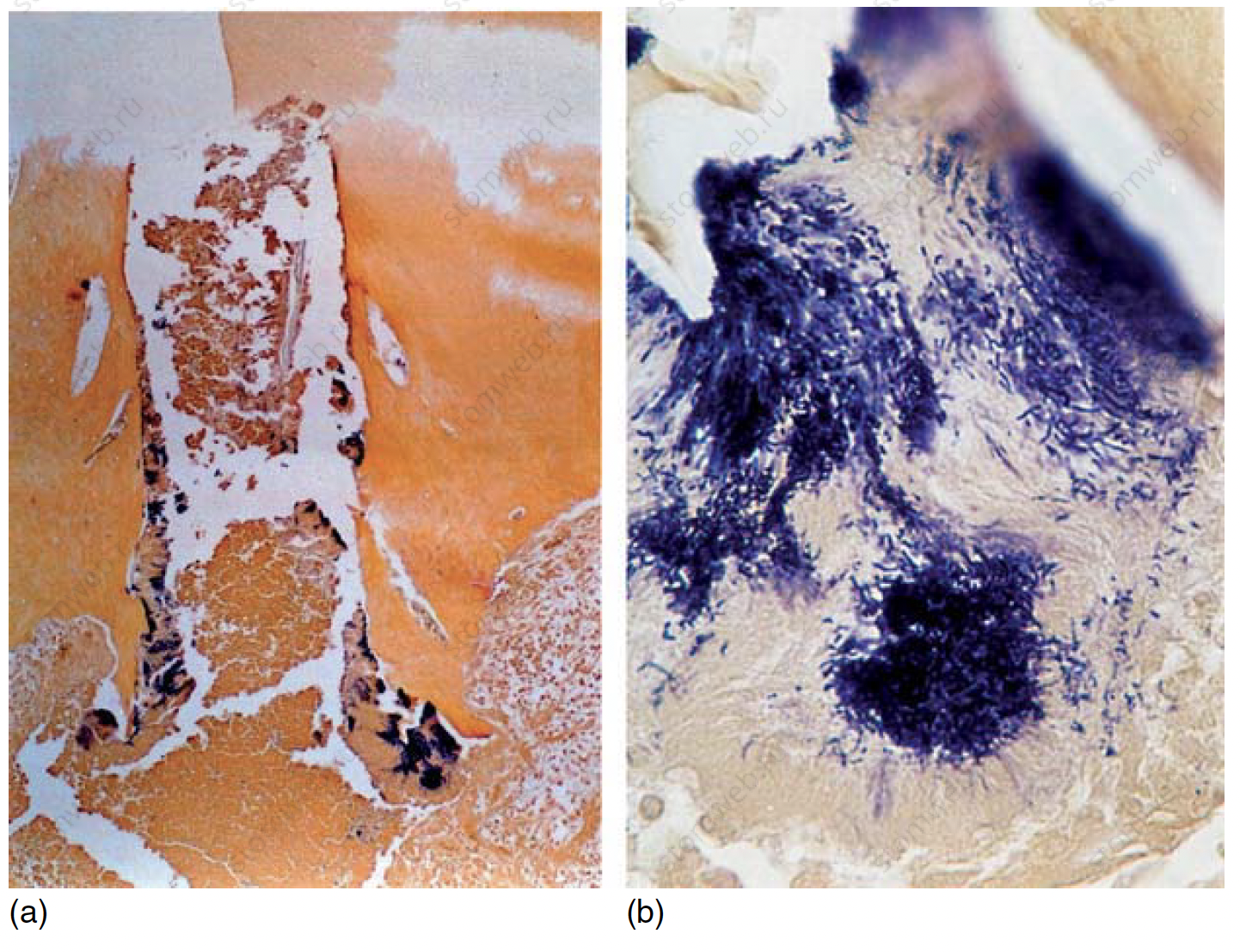
Рисунок 4 (а, b) Микроорганизмы, обнаруженные в разветвлениях апикальной дельты зубов с апикальным периодонтитом. Окрашивание по Брауну и Бренну.

Рисунок 5 Микроорганизмы, организованные в виде биопленок на внешних поверхностях апикальной трети корня. (а) Окрашивание по Брауну и Бренну.

Рисунок 5 Микроорганизмы, организованные в виде биопленок на внешних поверхностях апикальной трети корня. (b) Сканирующая электронная микроскопия.
Исторически в целях дезинфекции корневого канала между сеансами эндодонтического лечения использовались различные вещества и лекарства, в том числе пасты на основе гидроксида кальция, пасты с полиантибиотиками, трикрезол и формалин, камфорированный парамонохлорфенол и хлоргексидин сам по себе или в сочетании с другими веществами.
В то же время исследования постоянных зубов с использованием микробной культуры и биомолекулярных методов установили, что инфекция зубов с некрозом пульпы и апикальным периодонтитом имеет полимикробную природу с преобладанием анаэробных форм, преимущественно грамположительных бактерий. Подобные результаты также были полученыв исследованиях временных зубов.
Помимо выделения токсинов и продуктов метаболизма в ткани, грамположительные бактерии продуцирют эндотоксин клеточной стенки, также известный как ЛПС из-за его липополисахаридной природы. Это вещество представляет собой один из основных факторов вирулентности этих микроорганизмов. Бактериальный эндотоксин высвобождается после гибели или размножения микроорганизмов и вызывает ряд биологических реакций, которые активируют иммунокомпетентные клетки, которые выделяют провоспалительные цитокины и медиаторы, что обуславливает возникновение воспалительной реакции, остеокластогенез и резорбцию цемента и кости, таким образом способствуя возникновению (Рисунок 6), развитию и персистированиию апикального периодонтита. Также была обнаружена взаимосвязь между количеством бактериального эндотоксина в корневых каналах и присутствием клинических симптомов, таких как боль, чувствительность при перкуссии и пальпации, отек и гнойный экссудат.
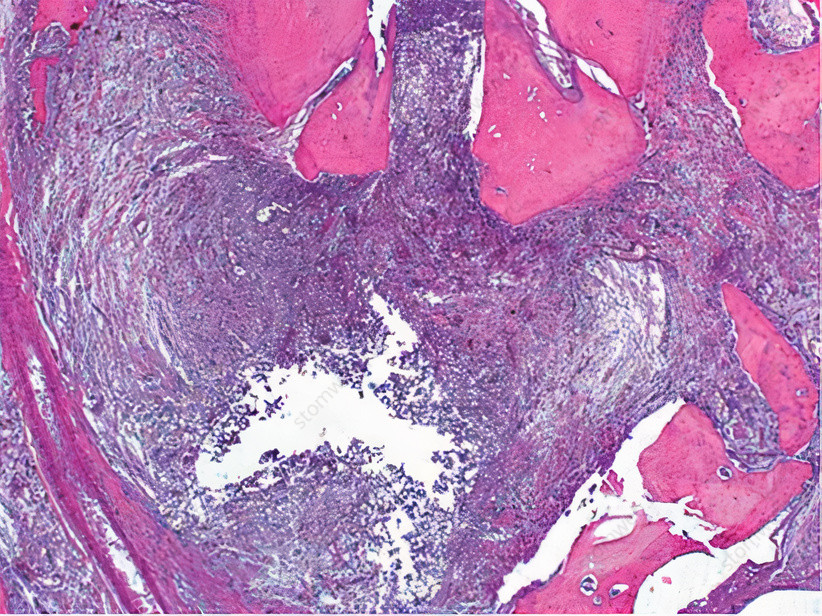
Рисунок 6 Апикальная воспалительная реакция и остеокластогенез, приводящие к развитию апикального периодонтита. Гематоксилин и эозин.
Давно известно, что эндотоксины бактерий могут стимулировать некоторые типы клеток организма-хозяина посредствам рецепторов, таких как липополисахарид-связывающий белок (LBP), рецептор CD14 и толл-подобные рецепторы (TLR), которые вызывают экспрессию провоспалительных цитокинов и усиливают имунный ответ. Бактериальный эндотоксин действует на макрофаги и другие типы клеток, стимулируя экспрессию фактора некроза опухоли (ФНО), интерлейкина-1, интерлейкина-6 и интерлейкина-8. Кроме того, бактериальный эндотоксин действует как потенциальный индуктор выработки оксида азота.
Бактериальный эндотоксин также активирует фактор Хагемана (фактор свертывания крови XII), метаболизм арахидоновой кислоты и систему комплемента, а также является пирогенным агентом, вызывающим лихорадку. Он участвует в воспалительных реакциях, таких как увеличение проницаемости сосудов, хемотаксиса нейтрофилов и макрофагов, а также высвобождения лизоцимов и лимфокинов. Было высказано предположение, что ЛПС-опосредованная сенсибилизация ноцицепторов является одним из механизмов, ответственных за боль, ассоциированную с эндодонтическими и апикальными инфекциями.
Помимо того, что бактериальный эндотоксин вызывает воспалительную реакцию, он прикрепляется к минерализованным тканям, стимулируя резорбцию кости, синтез и высвобождение цитокинов, активирующих остеокласты и остеокластогенез. Таким образом, в зубах с апикальным периодонтитом показано использование препаратов для временной пломбировки корневых каналов между сеансами лечения, чтобы помочь устранить эндодонтическую инфекцию и инактивировать бактериальный эндотоксин. Были проведены исследования материалов, обладающих антимикробной активностью, на предмет инактивации бактериального эндотоксина и других компонентов бактериальной клеточной стенки. Были исследованы гидроксид кальция, полимиксин B, формокрезол, хлоргексидин, Er:YAG-лазер, ультразвук, озонированная вода и гипохлорит натрия в разных концентрациях.
Вероятность присутсвия бактериального эндотоксина и жизнеспособных микроорганизмов в корневом канале на стадии пломбирования выше при проведении эндодонтического лечения в один сеанс. Теоретически, большая часть остаточных бактерий может быть уничтожена при контакте с пломбировочным материалом или остаться внутри дентинных канальцев, где погибнет от нехватки питательных веществ. Кроме того, учитывая сложную анатомию корневого канала, а также небольшое количество и низкую патогенность остаточных бактерий, предполагается, что выжившие микроорганизмы не способны добраться до периапикальных тканей. Однако следует учитывать, что корневые пломбы не обеспечивают апикальной и корональной герметизации против микроорганизмов. Кроме того, остаточные микроорганизмы могут достичь периапикальных тканей через границу между пломбировочным материалом и стенками канала, а также через дентинные канальцы, апикальный цемент и апикальные разветвления канала – дельты. Микроорганизмы также могут сохраняться после одноэтапного эндодонтического лечения в агрегатах, прилипших к поверхности цемента (апикальная биопленка). Таким образом, была продемонстрирована значительная корреляция между неудачами эндодонтического лечения и наличием остаточных микроорганизмов в обтурированных корневых каналах.
Традиционно лечение корневых каналов зубов с некротизированной пульпой и апикальным периодонтитом проводилось в несколько посещений с использованием внутриканальных препаратов, которые воздействуют на микроорганизмы в промежутках между приемами. Такой подход признан безопасным и эффективным. Идея завершения лечения корневых каналов зубов в одно посещение была предложена только для сокращения продолжительности лечения и основана на достижении аналогичных положительных результатов при клинических и рентгенографических оценках после односеансного лечения. Тем не менее, это все еще остается спорной темой в эндодонтической литературе, главным образом, учитывая относительно короткие периоды наблюдения в некоторых исследованиях. Кроме того, некоторые сторонники односеансного эндодонтического лечения считают частичное заживление периапикальных тканей бессимптомных зубов успехом, что увеличивает показатели успешности такого лечения.
Несомненно, персистенция апикального периодонтита или даже рентгенологические признаки частичного восстановления периапикальных тканей после лечения указывают на наличие остаточной инфекции в системе корневых каналов или на внешних апикальных поверхностях корня. Этот фактор может препятствовать полному заживлению, что приводит к сохранению хронического апикального воспалительного инфильтрата и образованию участков резорбции цемента и кости (Рисунок 7).
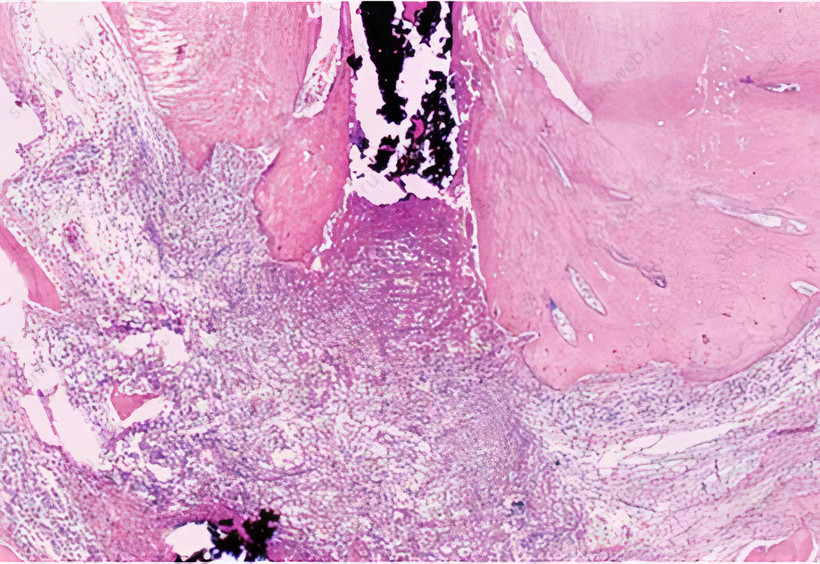
Рисунок 7 Персистенция апикального периодонтита после эндодонтического лечения. Высока вероятнось остаточной инфекции в системе корневых каналов или на внешних апикальных поверхностях корня. Гематоксилин и эозин.
Известно, что клинические проявления персистирующего апикального периодонтита могут не наблюдаться в течение нескольких месяцев или даже лет после лечения. Это состояние вместе с рентгенологическими признаками заживления (часто частичного) периапикальных тканей без восстановления компактной пластинки альвеолярной кости можно назвать эволюцией воспалительного процесса. На гистологическом уровне такой процесс нельзя назвать полным заживлением. При гистопатологическом анализе апикальные поражения с рентгенологическими признаками частичного заживления демонстрируют выраженную дезорганизацию тканей и сохранение воспалительных реакций.
Можно сделать вывод, что препараты для внутриканального применения должны обладать антисептическими свойствами и не оказывать неблагоприятного воздействия на периапикальные ткани, а также стимулировать регенеративные процессы.
Препараты для внутриканального применения – определение
Препараты для внутриканального применения можно охарактеризовать как лекарства или вещества для заполнения корневых каналов после биомеханической обработки между сеансами лечения для:
- нейтрализации бактериального эндотоксина, уничтожения и предотвращения размножения микроорганизмов в системе корневых каналов зубов с некротизированной пульпой и апикальным периодонтитом;
- снижения интенсивности периапикальных воспалительных явлений;
- создания физического и химического барьера, предотвращения повторного инфицирования канала и минимизации подтеканий через временную реставрацию;
- локального увеличения pH среды.
Необходимые свойства препаратов для временного пломбирования корневых каналов
Вещество или препарат для временного пломирования корневых каналов должны обладать следующими свойствами: